دانشنامه ریاضی و کامپیوتر
سایت جامع در باب کتب و جزوات رشته های ریاضی و کامپیوتر با دانلود مستقیم.
سایت جامع در باب کتب و جزوات رشته های ریاضی و کامپیوتر با دانلود مستقیم.
اوربیتال اتمی تابع ریاضی است که رفتار موجی مانند یک الکترون و یا یک جفت الکترون در اتم را توضیح میدهد..[۱] این تابع را میتوان به منظور محاسبهٔ احتمال حضور الکترون در یک اتم در مناطق خاصی در اطراف هسته مورد استفاده قرار داد. از عملکرد این تابع میتواند در ترسیم نمودار سه بعدی از احتمال حضور الکترون در یک مکان استفاده کرد که این منطقهٔ فیزیکی با احتمال زیاد تعیین میشود.[۲] به طور خاص، اوربیتالهای اتمی ممکن در ویژه حالتی از یک تک الکترون که در مجموعهای از الکترونها در اطراف اتم منفرد قرار دارند با تابع اوربیتال توضیح داد.
اوربیتال اتمی که در آن الکترون به عنوان ذرات جامد است را هرگز نمیتوان با سیارهٔ که بصورت بیضوی به دور خورشید میگردد توضیح داد.
روش چینش الکترون در اوربیتالهای یک اتم

با یک مقایسه دقیق ممکن است چنین به نظر برسد که الکترونی که درجو اطراف هسته قرار دارد مانند جو یک سیارهاست. اوربیتال اتمی نحوه شکل گیری این جو را فقط به یک الکترون منفرد در یک اتم را توضیح میدهد. وقتی که الکترونهای بیشتری به اتم منفرد اضافه میشود این الکترونها تمایل دارند بطور مساوی در حجم فضای اطراف هسته قرار بگیرند (که گاهی به این ابر الکترونی) گفته میشود.[۳])این منطقه معمولاً کروی شکل است.
این ایده که الکترون ممکن است در اطراف هسته با چرخشی که به آن تکانهٔ زاویهای می گویند در سال 1913 توسط نیلز بور استدلال شد.[۴] و یک فیزیکدان ژاپنی به نام (Hantaro Nagaoka) در اوایل سال 1904 فرضیه مبتنی به رفتارهای الکترونیکی به این مورد را منتشر کرد..[۵] با این حال تا سال 1926 معادله شرودینگر برای حل حرکت موجی الکترون در اتم برای توابع اوربیتال جدید آماده نبود..[۶]
با توجه به تفاوت مدارمکانیک کلاسیک از واژه «مدار» برای الکترون در اتم، برای اولین بارشیمیدانی بنام رابرت میلیکان در سال 1932 اصطلاح اوربیتال را ابداع و جایگزین آن کرد..[۷] اوربیتال اتمی، معمولاً به عنوان توصیف هیدروژنگونه (به معنی یک الکترون) برای تابع موج در فضا است، اعداد کوانتومی که بصورت n، l و m دسته بندی میشوند متناظر هستند با جفت الکترون انرژی، که تکانه زاویهای و تکانه زاویهای مسیر از آن به دست میآیند. هر اوربیتال (توسط یک مجموعه از اعداد کوانتومی متفاوت تعریف میشود) که دارای حداکثر دو الکترون است، از نامهای کلاسیک در آرایش الکترونی نشان داده شده در تصویر سمت چپ نیزاستفاده شدهاست. نامهای اوربیتال کلاسیک که با (s, p, d, f) نشان داده میشوند از ویژگیهای خطوط طیفی آنها مشتق شدهاست.[۸][۹]
از حدود سال 1920، یا حتی قبل از ظهور مکانیک کوانتومی مدرن، اصل آفبا (اصل ساخت و ساز) است که در آن اتمها متشکل از جفت الکترونهای هستند، که از تکرار یک الگوی ساده و منظم که با افزایش اعداد فرد (.. 1، 3، 5، 7) است پیروی میکنند، توسط نیلز بور و دیگران که برای پی بردن به وجود چیزی شبیه به اوربیتال اتمی، در داخل تعدادی از ساختار الکترونی اتمهای پیچیده مورد استفاده قرار گرفته بود. در ریاضیات فیزیک اتمی، برای ساده کردن تابع موج الکترون در سیستمهای پیچیده اغلب مناسب از ترکیبات ساده تر اوربیتال اتمی استفاده شود. اگرچه هر الکترون را نمیتوان در یک اتم چند الکترونی که یکی را از یک یا دوالکترون ازاوربیتال اتمی در یک تصویر خیالی محدود کرد، هنوز هم تابع موج الکترون ممکن است ترکیباتی از اوربیتال اتمی را دربر داشته باشد؛ مثل اینکه، در بعضی مواقع ابر الکترونی یک اتم چند الکترونی هنوز هم با اوربیتال اتمی متشکل از تنها یک یا دو الکترون باشد
نام گذاری اوربیتالها
اوربیتالها به فرم زیر نام گذاری میشوند:
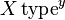
که در آن x مربوط به سطح انرژی برای عدد کوانتومی n است. Type مربوط به عدد کوانتومی دوم l که با (s, p, d, …) مشخص میشود است. و y مربوط به تعداد الکترونها در آن اوربیتال است.
برای مثال اوربیتال 1s2 (بخوانید یک اس دو) که دو الکترون دارد و سطح انرژی آن مربوط به n=1 (پایینترین سطح انرژی) است. و حرف s مربوط به l=0 است. در نماد اشعه ایکس، عدد کوانتومی اصلی آن با حروفی وابسته به اعداد نام گذاری میشود. برای n=1, 2, 3,.. که حروف معادل آنها که به ترتیب با K, L, M, N, O,... نشان داده میشود.
در مکانیک کوانتومی، حالت یک اتم، یعنی حالتهای انرژی با هامیلتونی آن اتم، گسترش مییابد (که توسعه آن با کاربرد جبر خطی پایهاست) که حاصل ترکیبات خطی پاد متقارن توابع تک الکترونی (دترمینان اسلیتر) است. قسمت فضایی تابع تک الکترونی را اوربیتال اتمی مینامند.
در فیزیک اتمی، خطوط طیفی اتم با انتقال (پراش کوانتومی) بین ویژه حالتهای یک اتم ایجاد میشود. این حالتها توسط یک مجموعه از اعداد کوانتومی برچسب گذاری میشود، خلاصه از نماد کوتاهی که برای آرایش الکترونی که شکل آن برای نمونه برای اتم نئون بصورت (1s2 2s2 2p6)است استفاده میشود.
معمولا در این نماد خصوصیات ظاهری وشکل تداخلی توضیح داده میشود. مفهوم اوربیتال اتمی از یک تجسم برای یک فرایند مربوط به تحریک به حالت گذار است. به عنوان مثال، با تحریک کردن یک الکترون از یک اوربیتال به یک اوربیتال خالی فرایند گذار انجام میشود. باید به این نکته توجه داشت که برای الکترونهای فرمیون اصل طرد پاولی بر آنها حاکم است. و نمیتوان آنها را از سایر اکترونهای اتم متمایز کرد. علاوه بر این، ممکن است بعضی وقتها اتفاق بافتد که نتوان از شکل تداخلی برای تعیین یک تابع موج ساده صحبت کرد که این مورد برای ارتباط الکترونی بزرگ است. اساساً تابع موج برای سیستم تک الکترونی است برای سیستمهای چند الکترونی ما برای این مورد از یک تقریب سیستم تک الکترونی استفاده میکنیم. برای این تقریب ما از تقریب (Hartree–Fock) استفاده میکنیم که این تقریب پیچیدگیهای تئوری اوربیتال مولکولی را نیز کاهش میدهد.
بلافاصله پس از هایزنبرگ رابطه عدم قطعیت که توسط بور موجودیت یافته بود فرمول بندی شد، که در هر نوع بسته موجی دلالت بر عدم قطعیت در فرکانس و طول موج بود، از آن به بعد انتشارفرکانسها منوط به ایجاد یک بسته برای خود شده بود. در مکانیک کوانتومی، ممان تمام ذرات به امواج وابسته هستند، در شکل گیری چنین بسته موجی از متمرکز کردن ذرات موجود در فضا برای یک موج استفاده میشود. در هر جای مکانیک کوانتومی ذرات محدود به ویژه حالتها هستند، که باید در یک بسته موج متمرکز شوند، و وجود بستهها و اندازه مینیمم آنها دلالت برانتشار و مقدار حداقلی آن در طول موج ذرات است، و همچنین با تکانه و انرژی با مقدار حداقلی طول موج ذرات در ارتباط است. در مکانیک کوانتومی، ذراتی که در یک منطقه کوچکی از فضا محدود هستند، در متراکم بودن و وابستگی بستهٔ موج نیاز به گسترهٔ بزرگی از ممان است که بنابراین آن همان بزرگی انرژی جنبشی است. بنابراین انرژی بستگی که حاوی یا ذراتی که در ناحیهٔ کوچک از فضا گیرانداخته شدهاند بدون محدودیت افزایش مییابند و این رشد کمتر آن ناحیه را در بر دارد. ذرات نمیتوانند در یک نقطه هندسی محصور باشند. چونکه بی نهایت ذره داریم.
در شیمی افرادی مانند شرودینگر، پاولی، میلیکان و دیگران اشاره به این کردند که در رابطه هایزنبرگ الکترون به عنوان بسته موج، نمیتواند در یک مکان دقیق در اوربیتال در نظر گرفته شود. ماکس بورن پیشنهاد کرد که موقعیت الکترون را میتوان با یک توزیع احتمال توصیف کرد که برای پیدا کردن الکترون باید به تعداد زیادی از نقطهها متوصل شد که وابستگی بسته موج با تابع موج توضیح داده میشود. در مکانیک کوانتومی جدید نتیجه دقیقی به ما نمیدهد، اما این تنها احتمالات است که وقوع نتایج گوناگونی را ممکن کردهاست. هایزنبرگ میانگاشت که مسیر حرکت الکترون معنی ندارد اگر ما نتوانیم آنرا مشاهده کنیم همچنان که با الکترونهای یک اتم نمیتوانیم.
در اثر کوانتومی هایزنبرگ، شرودینگر و دیگران عدد اتمی بور (n) برای هر اوربیتال شناخته شده و کرهٔ در یک اتم سه بعدی و اثر انرژی متوسط بر احتمال، میتواند الکترونهای بستهٔ موج یک اتم را احاطه کنند.
اگرچه هایزنبرگ برای موقعیت الکترون از بی نهایت مجموعه برای ماتریس اش استفاده کرد، این به این معنی نبود که الکترون نمیتواند در هیچ جای جهان باشد. بلکه این قوانین نشان میدهد که الکترون باید در توزیع احتمال متمرکز شود. در یک الکترون توصیف انرژی آن با مکانیک ماتریسی حساب میشود. از اینرو، الکترون در یک کره معین با یک گستره معین به انرژی مربوط به هسته وابستهاست که محدود به این مکان است.
اتمهای هیدروژن گونه سادهترین اوربیتالهای اتمی هستند که با یک الکترون مانند اتم هیدروژن رخ میدهد. در این صورت اوربیتالهای اتمی از حالتهای انرژی هامیلتونی اتم هیدروژن هستند. که با تحلیل و تجزیه به دست میآیند (مانند اتم هیدروژن). یونیزاسیون عنصر اتم دیگری که با تک الکترون شبیه اتم هیدروژن است که همان فرم را میگیرد.
برای اتمهای که با دو یا چند الکترون هستند، معادلات حاکم برآنها فقط میتوانند با استفاده از روشهای تقریبی متوالی حل شوند. اوربیتالهای اتمی که چند الکترونی هستند از لحاظ کیفی شبیه به هیدروژن هستند و از مدلهای ساده تبعیت میکنند و همان فرم را میگیرند.
برای آنالیزهای دقیق و پیچیده از تقریبهای عددی استفاده میشود.
برای اوربیتال یک اتم معین (هیدروژن گونه) از سه شناسهٔ عددهای کوانتومی (n ,l, ml) و مقادیر منحصربفرد مربوط به آنها استفاده میشود. محدود کردن اعداد کوانتومی و انرژی مربوط به آنها نحوه آرایش الکترونی اتمها و جدول تناوبی را توضیح میدهد.
وضعیت سکون (ویژه حالتهای) اتمهای هیدروژن گونه همان اوربیتال اتمی هستند. هر چند در طبیعت رفتار الکترونها را نمیتوان کاملاً با تک اوربیتال توضیح داد.
نخستین عدد کوانتومی n در مدل بور دیده میشود. از جمله چیزهای دیگر را که تعیین میکند مانند فاصله الکترون از هستهاست. همه الکترونها با همان مقدار n و در همان فاصله واقع میشوند. مکانیک کوانتومی مدرن این اوربیتالها را با دقت وابستگی زیاد تثبیت میکند. برای این دلیل اوربیتالها با همان مقدار n که شامل «پوسته» است بیان میشود. اوربیتالهای که با مقدار n و l زوج هستند بیشتر برای دقت وابستگی آنها با زیرپوسته بیان میشود.
اوربیتال اتمی به طور خاص با مقادیر سه عدد کوانتومی شناخته میشود و هر مجموعهای از سه عدد کوانتومی دقیقا به یک اوربیتال مربوط میشود، اما اعداد کوانتومی تنها تحت شرایط و مقادیرمعینی با یکدیگر ترکیب میشوند.. قوانین حاکم بر مقادیر ممکن اعداد کوانتومی عبارتند از:
عدد کوانتومی اصلی n، همیشه عدد صحیح مثبتی است. در واقع، میتواند هر عدد صحیح مثبتی باشد، ولی بنا به دلایلی که در ادامه مورد بحث قرار میگیرند، به ندرت با اعداد بزرگ مواجه میشویم.هر اتم در کل اربیتالهای زیادی بسته به هر مقدار n دارد؛ این اوربیتالها با یکدیگر گاهی لایههای الکترونی نامیده میشوند.
عدد کوانتومیazimuthal (سمتی یا اوربیتالی)  عدد صحیح غیر منفی است. اگر عدد کوانتومی اصلی، عدد صحیح n0 باشد
عدد صحیح غیر منفی است. اگر عدد کوانتومی اصلی، عدد صحیح n0 باشد  میتواند هر مقداری که در شرط
میتواند هر مقداری که در شرط  صدق میکند، باشد. به عنوان مثال، برای n = 1 لایه فقط اوربیتال
صدق میکند، باشد. به عنوان مثال، برای n = 1 لایه فقط اوربیتال 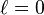 وبرای n = 2 لایه فقط اوربیتالهای، و را خواهد داشت. مجموعهای از اوربیتالهای در ارتباط با یک مقدار خاص از گاهی در مجموع زیر لایه(subshell) نامیده میشوند.
وبرای n = 2 لایه فقط اوربیتالهای، و را خواهد داشت. مجموعهای از اوربیتالهای در ارتباط با یک مقدار خاص از گاهی در مجموع زیر لایه(subshell) نامیده میشوند.
عدد کوانتومی مغناطیسی 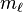 همواره یک عدد صحیح است. درون زیرپوستهای (subshell)که در آن
همواره یک عدد صحیح است. درون زیرپوستهای (subshell)که در آن  عددصحیح
عددصحیح 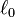 است،
است، 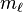 هایی که در شرط مقابل صدق کنند، وجود دارند:
هایی که در شرط مقابل صدق کنند، وجود دارند: 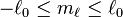 .
.
نتایج فوق را میتوان در جدول زیر خلاصه کرد. هر خانه نشان دهنده یک زیرلایهاست، و لیست مقادیر مجاز 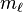 در آن خانه جای گرفتهاند.اوربیتال محدودهای از فضای اطراف هسته میباشد که احتمال یافتن الکترون در آن وجود دارد. این احتمال در نزدیکی هسته بیشترین مقدار را دارد. ولی برای تمام نقاطی از فضا که فاصله معینی از هسته دارند، احتمال معینی وجود دارد. هر اوربیتال میتواند حداکثر دو الکترون را در خود جای دهد. دو الکترونی که در یک اوربیتال جای میگیرند، دارای اسپین مخالف هستند.
در آن خانه جای گرفتهاند.اوربیتال محدودهای از فضای اطراف هسته میباشد که احتمال یافتن الکترون در آن وجود دارد. این احتمال در نزدیکی هسته بیشترین مقدار را دارد. ولی برای تمام نقاطی از فضا که فاصله معینی از هسته دارند، احتمال معینی وجود دارد. هر اوربیتال میتواند حداکثر دو الکترون را در خود جای دهد. دو الکترونی که در یک اوربیتال جای میگیرند، دارای اسپین مخالف هستند.
هر الکترون را میتوان با چهار عدد کوانتومی مشخص کرد که به منزله شناسنامه الکترون هستند و فاصله نسبی الکترون از هسته (n)، لایه فرعی و شکل اوربیتال (L)، جهت گیری اوربیتال در فضا (s) را بیان میکنند. بر اساس اصل طرد پاولی در یک اتم هیچ دو الکترونی را نمیتوان یافت که تمام چهار عدد کوانتومی آنها یکسان باشد.
 | 1 | 2 | 3 | 4 | ... | |
|---|---|---|---|---|---|---|
 |
 |
|||||
| 2 | 0 | -1, 0, 1 | ||||
| 3 | 0 | -1, 0, 1 | -2, -1, 0, 1, 2 | |||
| 4 | 0 | -1, 0, 1 | -2, -1, 0, 1, 2 | -3, -2, -1, 0, 1, 2, 3 | ||
| 5 | 0 | -1, 0, 1 | -2, -1, 0, 1, 2 | -3, -2, -1, 0, 1, 2, 3 | -4, -3, -2 -1, 0, 1, 2, 3, 4 | |
| ... | ... | ... | ... | ... | ... | ... |
زیر لایه هامعمولا با مقادیر - و -
و - خود شناخته میشوند.
خود شناخته میشوند.  با مقدار عددی آن نشان داده شدهاست.و برای هر
با مقدار عددی آن نشان داده شدهاست.و برای هر  ، در خانههای مربوط به
، در خانههای مربوط به  هایی که میتواند داشته باشد،
هایی که میتواند داشته باشد،  های مربوط به آن
های مربوط به آن  نمایش داده شدهاند.اربیتال 0 با حرف s، اربیتال 1باحرف p، اربیتال 2 با حرف d، اربیتال 3 با حرف f و اربیتال4 با حرف g نمایش داده میشوند. به عنوان مثال اربیتال 0 مربوط به در n = 2 به صورت 2s نشان داده میشود.
نمایش داده شدهاند.اربیتال 0 با حرف s، اربیتال 1باحرف p، اربیتال 2 با حرف d، اربیتال 3 با حرف f و اربیتال4 با حرف g نمایش داده میشوند. به عنوان مثال اربیتال 0 مربوط به در n = 2 به صورت 2s نشان داده میشود.
هر بحثی در مورد شکل اوربیتال الکترون ضرورتا نا درست است، زیرا یک الکترون بدون در نظر گرفتن اینکه مداری را اشغال میکند، میتواند به علت اصل عدم قطعیت در هر لحظه در هر فاصله از هسته و در هر مسیری یافت شود.

با این حال، الکترون در مناطق خاصی بااحتمال بیشتری نسبت به مناطق دیگر یافت میشود. با توجه به این مساله، میتوان سطحی را در نظر گرفت که نقاط داخل سطح با احتمال بالا را از نقاط خارجی که احتمال کمتری دارند جدا سازد. جایگذاری دقیق سطح، قراردادی وفرضی است، اما اگر این سطح معقولانه انتخاب شود باید از الگویی که رفتار مربع تابع موج 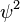 مشخص میکند، پیروی کند.این سطح مرزی آن چیزی است شکل اربیتال نامیده میشود. به طور کلی، عدد کوانتومی اصلی n برای یک هسته مشخص، اندازه و انرژی اربیتال رامشخص میکند. افزایش n، اندازه اربیتال را افزایش میدهد. با این حال، در مقایسه عناصر مختلف، بار مثبت (عدد اتمی که تعداد پروتونها را میرساند) بیشتردر عناصر سنگین باعث انقباض اوربیتالها در مقایسه با عناصر سبک میشودو به این دلیل اندازه کلی اتم ثابت میماند(با وجود اینکه تعداد الکترونها در عناصر سنگین تر افزایش مییابد). همچنین به صورت کلی،
مشخص میکند، پیروی کند.این سطح مرزی آن چیزی است شکل اربیتال نامیده میشود. به طور کلی، عدد کوانتومی اصلی n برای یک هسته مشخص، اندازه و انرژی اربیتال رامشخص میکند. افزایش n، اندازه اربیتال را افزایش میدهد. با این حال، در مقایسه عناصر مختلف، بار مثبت (عدد اتمی که تعداد پروتونها را میرساند) بیشتردر عناصر سنگین باعث انقباض اوربیتالها در مقایسه با عناصر سبک میشودو به این دلیل اندازه کلی اتم ثابت میماند(با وجود اینکه تعداد الکترونها در عناصر سنگین تر افزایش مییابد). همچنین به صورت کلی،  شکل مدارو
شکل مدارو 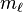 جهت گیری آنرا مشخص میکند. با این حال، چون برخی از اوربیتالها توسط معادلاتی در اعداد مختلط تعریف میشوند، گاهی اوقات شکل اوربیتال به
جهت گیری آنرا مشخص میکند. با این حال، چون برخی از اوربیتالها توسط معادلاتی در اعداد مختلط تعریف میشوند، گاهی اوقات شکل اوربیتال به 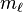 نیز بستگی پیدا میکند.
نیز بستگی پیدا میکند.
اوربیتال s تنها (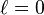 ) شکلی کره مانند دارد. برای n=1، این اوربیتال مانند کرهای توپر (با چگالی بالا وشکلی متقارن) است، اما برای ñ = 2 یا بیشتر، اوربیتالهای s از کرههای متقارنی که پوستههای تو در تویی هستند تشکیل یافتهاست.هر یک (به عنوان مثال، ساختار موج، شعاعی است و مطابق یک مولفه شعاعی سینوسی). اوربیتالهای s تنها اوربیتالهایی هستند که برای همه nها دارای یک ((شکم)) در مرکز هسته میباشند.(منطقهای که چگالی تابع موج در آن بالا باشد شکم نامیده میشود). - همه اوربیتال دیگر (p، d، f و غیره) تکانه زاویهای دارند، و در نتیجه از هسته دوری میکنند (داشتن یک گره در هسته به این دلیل است).
) شکلی کره مانند دارد. برای n=1، این اوربیتال مانند کرهای توپر (با چگالی بالا وشکلی متقارن) است، اما برای ñ = 2 یا بیشتر، اوربیتالهای s از کرههای متقارنی که پوستههای تو در تویی هستند تشکیل یافتهاست.هر یک (به عنوان مثال، ساختار موج، شعاعی است و مطابق یک مولفه شعاعی سینوسی). اوربیتالهای s تنها اوربیتالهایی هستند که برای همه nها دارای یک ((شکم)) در مرکز هسته میباشند.(منطقهای که چگالی تابع موج در آن بالا باشد شکم نامیده میشود). - همه اوربیتال دیگر (p، d، f و غیره) تکانه زاویهای دارند، و در نتیجه از هسته دوری میکنند (داشتن یک گره در هسته به این دلیل است).
سه اوربیتال p برای n=2 به صورت دوبیضی که در هسته به یکدیگر مماس میباشند (یابه عبارت، دیگر دمبلی شکل) هستند.هر یک از سه اوربیتال p هر لایه به صورت عمود بر دواوربیتال دیگر قرار گرفتهاست و هر یک، توسط مقدار 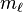 خود تعیین میشود.
خود تعیین میشود.
چهار اوربیتال ازپنج اوربیتال مربوط به d برای n=3 مشابه هستند. هر یک با چهار توپ گلابی شکل مشخص میشوند.هر یک توپ مماس بر دو توپ دیگر است، و مراکزهر چهار تا درصفحهای بین یک جفت محورقرار دارد(برای مشخص کردن هر صفحهای، دو خط متقاطع نیاز است). سه صفحه از این چهار صفحه، صفحات ý x، x ž و ý Ž هستند، و چهارمین صفحه مراکزی روی محورهای x و ý دارد.پنجمین و آخرین اوربیتال d متشکل از سه منطقه با چگالی احتمال زیاداست : چنبرهای دومنطقه گلابی شکل که به صورت متقارن روی محور Ž قرار گرفتهاست.
هفت اوربیتال f، هر یک اشکالی پیچیده تر از شکلهای اوربیتالهای d دارند.
برای هر مجموعه s، p، d، f ویا g از اوربیتالها که در آرایش الکترونی شرکت داشته باشند، آرایش به فرم مجموعه ای متقارن و کروی شکل در خواهد آمد. و برای اوربیتالهای غیر s، که { lobes }دارند، { lobe }ها در جهتی قرار میگیرند که فضا رابرای آن تعداد از ناحیهها که در هر مجموعهای از جهتها وجود دارند تا حد امکان به طورمتقارن ترپر کنند. به عنوان مثال، سه اوربیتال p شش ناحیه دارند که هر یک دریکی از شش جهت اصلی از 3 راستای فضای سه بعدی هستند؛ برای 5 اوربیتال d، در مجموع 18 ناحیه، وجود دارد که در آن دوباره شش ناحیه درراستای شش جهت اولیه، و 12 ناحیه بعدی 12 راستا را که بین هر جفت از این 6 محور اصلی وجود دارد، پر میکنند.
علاوه بر این، چنانکه موردی با اوربیتال s است اوربیتالهای p، d، f و g منحصر به فرد با مقادیر ñ بیشتر از پایینترین مقدار ممکن، ساختار گرهی شعاعی اضافی نمایان میشودکه یاد آور موجهای هارمونیک همان نوع با مد پایه موج است. مطابق با اوربیتال s در بالاترین مقدار ممکن بعدی ñ، دراوربیتالهای p، d، f و g (به عنوان مثال، در مقابل اوربیتالهای 2p پایه، اوربیتالهای 3p)، یک گره اضافی در هر لوب ایجاد میشود. برای هر نوع اوربیتالی مقادیر بالاتر ñ تعداد گرههای شعاعی را بیشتر افزایش میدهند.
شکل اوربیتالهای اتمی، در یک اتم تک الکترون به هماهنگهای کروی سه بعدی مربوط میشود.
این جدول پیکر بندی همه اوربیتالها رابرای توابع موج هیدروژن گونه تا اوربیتال 7s نشان میدهد و در نتیجه پیکربندیهای الکترونی ساده را برای همه عناصر در جدول تناوبی تا رادیوم پوشش میدهد.
| s (l=0) | p (l=1) | d (l=2) | f (l=3) | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| m=0 | m=0 | m=±1 | m=0 | m=±1 | m=±2 | m=0 | m=±1 | m=±2 | m=±3 | |||||||
| s | pz | px | py | dz2 | dxz | dyz | dxy | dx2-y2 | fz3 | fxz2 | fyz2 | fxyz | fz(x2-y2) | fx(x2-3y2) | fy(3x2-y2) | |
| n=1 |  |
|||||||||||||||
| n=2 |  |
 |
 |
 |
||||||||||||
| n=3 |  |
 |
 |
 |
 |
 |
 |
 |
 |
|||||||
| n=4 |  |
 |
 |
 |
 |
 |
 |
 |
 |
|||||||
| n=5 |  |
 |
 |
 |
 |
 |
 |
 |
 |
... | ... | ... | ... | ... | ... | ... |
| n=6 |  |
 |
 |
 |
... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... |
| n=7 |  |
... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... |
در اتمی با یک الکترون منفرد (اتمهای هیدروژن گونه)، انرژی هر اوربیتال (و به تبع آن، انرژی هر الکترون در اوربیتال) منحصرا توسط  تعیین میشود.اوربیتال
تعیین میشود.اوربیتال  کمترین میزان انرژی ممکن را در اتم دارد. هر یک از مقادیرمتوالی بالاتر
کمترین میزان انرژی ممکن را در اتم دارد. هر یک از مقادیرمتوالی بالاتر  سطح انرژی بالاتری دارند، اما اختلاف انرژیها با افزایش
سطح انرژی بالاتری دارند، اما اختلاف انرژیها با افزایش  کاهش مییابد. برای
کاهش مییابد. برای  بزرگ، سطح انرژی به حدی زیاد است که الکترونها به آسانی میتواند از اتم فرار کنند.
بزرگ، سطح انرژی به حدی زیاد است که الکترونها به آسانی میتواند از اتم فرار کنند.
در اتمهای با الکترونها ی بیشتر، انرژی الکترون نه تنها از خواص ذاتی اوربیتال آن است، بلکه به بر هم کنش با الکترونهای دیگرنیز بستگی دارد. این بر هم کنشها به جزئیات توزیع احتمال مکانی آن الکترون بستگی دارد، و بنابراین سطح انرژی اوربیتالها نه تنها به  بستگی دارد، بلکه به
بستگی دارد، بلکه به  نیز وابستهاست. مقادیر بالاتر از
نیز وابستهاست. مقادیر بالاتر از  مقادیر بالاتری از انرژی همراه خواهند شد؛ به عنوان مثال، حالت p2 انرژی بیشتری از حالت s2 دارد. وقتی که
مقادیر بالاتری از انرژی همراه خواهند شد؛ به عنوان مثال، حالت p2 انرژی بیشتری از حالت s2 دارد. وقتی که  = 2 است انرژی اوربیتال به قدری افزایش مییابد که انرژی اوربیتال، به انرژی بالاتر ازانرژی اوربیتال s لایه بالاتر میرسد(رانده میشود)؛ هنگامی که
= 2 است انرژی اوربیتال به قدری افزایش مییابد که انرژی اوربیتال، به انرژی بالاتر ازانرژی اوربیتال s لایه بالاتر میرسد(رانده میشود)؛ هنگامی که  = 3 است انرژی به سطح انرژی دو مرحله بالاتر رانده شدهاست.
= 3 است انرژی به سطح انرژی دو مرحله بالاتر رانده شدهاست.
ترتیب انرژی 24 زیر لایه اول جدول زیر داده شدهاست. هر خانه نشان دهنده یک زیر لایهاست که با n و  مربوطه مشخص میشود.عدد داخل هر خانه نشان دهنده رتبه انرژی آن زیر لایه نسبت به سایر زیر لایهها است.
مربوطه مشخص میشود.عدد داخل هر خانه نشان دهنده رتبه انرژی آن زیر لایه نسبت به سایر زیر لایهها است.
 | 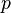 | 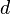 |  |  | |
|---|---|---|---|---|---|
| 1 | 1 | ||||
| 2 | 2 | 3 | |||
| 3 | 4 | 5 | 7 | ||
| 4 | 6 | 8 | 10 | 13 | |
| 5 | 9 | 11 | 14 | 17 | 21 |
| 6 | 12 | 15 | 18 | 22 | 26 |
| 7 | 16 | 19 | 23 | 27 | 31 |
| 8 | 20 | 24 | 28 | 32 | 36 |
توجه :خانههای خالی زیر لایههایی را که موجود نیستند نشان میدهند، در حالی که خانههایی که اعدادشان ایتالیک نوشته شدهاند زیر لایههایی هستند که میتوانند وجود داشته باشند اما در هیچ یک از عناصر شناخته شده فعلی قادر به نگه داشتن الکترونها نیستند.
قوانین زیادی بر چینش الکترونها در اوربیتال حاکمند نخستین قاعده این است که هیچ دو الکترونی در اتم نباید دارای مجموعهای مشابه از اعداد کوانتومی باشند(این اصل طرد پاولی است). اعداد کوانتومی شامل سه عددی که اوربیتال هارا تعریف میکنند به علاوه s یا عدد کوانتومی اسپین میشوند. بنابراین، دو الکترون ممکن است اوربیتال یکسانی را اشغال کنند که البته این امر وقتی ممکن است که مقادیر s متفاوتی داشته باشند. با این حال، تنها دو الکترون.به این دلیل که اسپینهای آنها میتواند با هر اوربیتال {ارتباط} بر قرار کند.
علاوه بر این، الکترون همیشه تمایل